|
Эванса Оксазолидоны в асимметрическом алкилировании (Evans Oxazolidinones) спасибки Thomas Ball (Pembroke) |
|
Оксазлидоны Эванса нашли широчайшее применение в качестве вспомогательных реагентов в синтезе карбоновых килот и их производных. Оксазолидоны обычно получают из легкодоступных аминокислот, таких как валин или фенилаланин. |
|
Общая схема и механизм
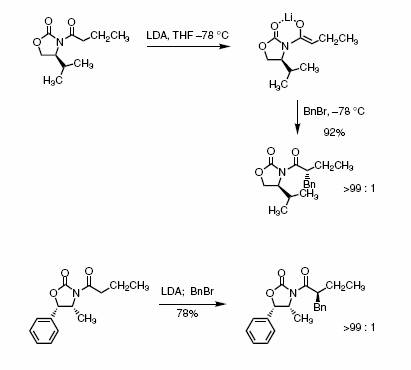
-При реакция с основанием и последующем алкилировании возникает новый асимметрический
центр в молекуле, который остается неизменным при последующем гидролизе до
карбоновой кислоты. -Z-Еноляты образуются с высокой
селективностью. Хелатация предполагается в переходном состоянии и в исходном. -Менее
реакционноспособные (не аллильные\бензильные) электрофилы требуют
использования более активных натриевых енолятов или трифлата как хорошей
уходящей группы. Пример рекции: Эта реакция, типичный пример использования оксазолидонов Эванса. Аллилирование происходит со стороны противоположной заместителю оксазалидиновогокольца. Стереоселективность зависит от выбора противоиона т.е. Li и K являясь кислотами Льюиса могут произвести контроль хелатированием, в то время как Na не является кислотой Льюиса и доминирующий фактор уменьшение неблагоприятных взаимодействий между паралельными C=O диполями Пример методики: Organic Syntheses, Coll. Vol. 8, p.528 (1993); Vol. 68, p.77 (1990). ссылка (Лиганд)
|
|
Ссылки 1. 1. Evans, D.A et al.; J.Am.Chem.Soc; 1988;
110; 2506 1. Первая публикация: Evans, D. A.; Ennis, M. D.; Mathre, D. J. J. Am. Chem. Soc. 1982, 104, 1737-1739. 2. Обзоры: D. A. Evans, Aldrichimica Acta 1982, 15(2), 23-32. link (b) Y. Gnas, F. Glorius Synthesis, 2006, (12), 1899-1930. 3. Механизм: |
|
Современные примеры использования оксазолидонов Эванса в асимметрическом алкилировании: |
|
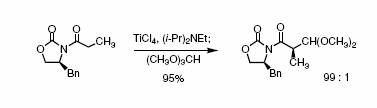
Примечание.Еноляты титана позволяют диастереоселективно
получить продукты сочетаний Sn1 типа. Ссылки: Evans, D. A.; Urpi, F.; Somers, T. C.; Clark, J. S.; Bilodeau, M. T. J. Am. Chem. Soc. 1990, 112, 8215-8216. |
|
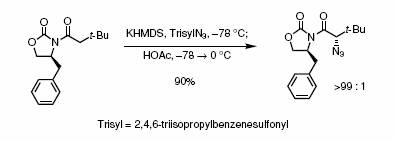
Примечание: Использование тризилазида в качестве нуклеофила позволяет получать аминокислоты после последующего восстановления азида до аминогруппы. Ссылки: D. A. Evans, T. C. Britton, J. A. Ellman, R. L. Dorow, J. Am. Chem. Soc. 1990, 112, 4011-4030. |
|
Примечание: Алкилированные оксазолидины можно также превращать в спирты, прямым восстановлением. Ссылки: Evans, D. A.; Bender, S. L.; Morris, J. J. Am. Chem. Soc. 1988, 110, 2506-2526. |