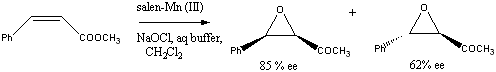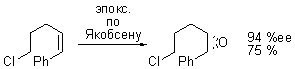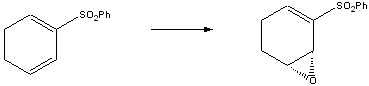|
Эпоксидирование по Якобсену (Jacobsen Epoxidation) спасибки Jeni Tod |
|
Коммерчески доступный катализатор Якобсена был назван реагентом 1994 года. Катализатор Якобсена переводит ахиральные олефины в хиральные эпоксиды с е.е. регулярно лучше 90%. Катализатор якобсена один из класса катализаторов эпоксидирования (более 75 известно ) на основе саленовых комплексов Mn(III). |
|
Схема и механизм: Общая схема и механизм
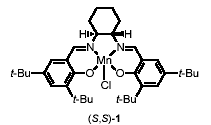
Катализатор Якобсена, молекула 1994 года:
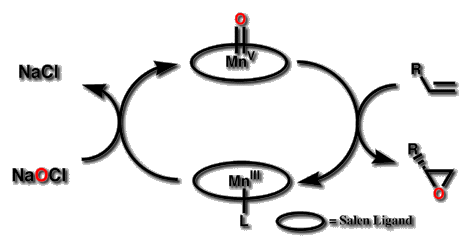
Каталитический цикл при этом выглядит так:
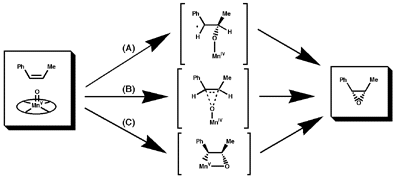
а для механизма предложены три следующие схемы:
• Селективность определяется невалентными
взаимодействиями! (nonbonded interactions). • Сопряженные цис-олефины окисляются с высокой энантиоселективностью. • транс-олефины реагируют медленнее и с меньшей селективностью. • В основном, R это арил, алкенил или алкинил и R' объемный заместитель. -терминальные и транс- олефины плохие субстраты -прибавление стехиометрического количества 4-фенилпиридиноксида улучшает селективность и каталитический выход.
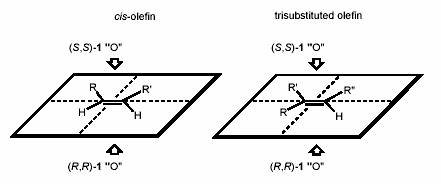
Для определения селективности: цис-олефины: Поместите арил, алкенил или алкинил в левый верхний
квадрат и поместите транс-водород в нижний правый квадрат Трехзамещенные
алкены: Поместите водород в нижний
правый квадрат.
Пример Простой пример использования хиральных
саленовых комплексов для
асимметрического эпоксидирования. |
|
Показательная методика: Катализатор: Organic Syntheses, Coll. Vol. 10, p.96 (2004); Vol. 75, p.1 (1998). linkЭпоксидирование:
Organic Syntheses, Coll. Vol. 10, p.29 (2004); Vol. 76, p.46
(1999). link |
|
Ссылки:
|
|
Использование эстерификации Кита в современной литературе: |
|
Примечание: Цис-эпоксид, послуживший исходным для синтеза (2S,3S)-3-гидрокси-2-фенилпиперидина, был получен с прекрасной энантиомерной чистотой посредством эпоксидирования по Якобсену. Ссылка: J. Lee, T. Hoang, S. Lewis, S. A. Weissman, D. Askin, R. P. Volante, P. J. Reider, Tetrahedron Letters 2001, 42(36), 6223-6225. link |
|
Примечание: В синтезе аналогов Stereotetradsan эпоксидирование по Якобсену было использовано на ранних стадиях. Ссылка: Org. Lett., 4 (21), 3571 -3574, 2002. другие современные именные реакции на главную |