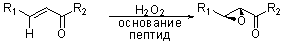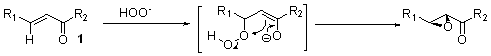|
Реакция Жюлиа-Колонна (Julia-Colonna epoxidation) (возм. синонимы Юлия-Колонна, Юлии-Колонна эпоксидирование) спасибки С. М. Робертсу |
|
Реакцией Жюлиа-Колонна называют асимметрическое эпоксидирование хальконов с помощью перекиси водорода и основания, катализируемое синтетическими полипептидами. Высокая стереоселективность (до 98 %ee) и обширная химия эпоксикетонов, продуктов реакции, стимулирует интерес к данной реакции. |
|
Схема и механизм:
R1 = арил, и R2 = арил, алкил, алкенил. основание = NaOH, DBU. полипетид = поли-L-лейцин, поли-D-лейцин, поли-D-аланин. Две самые популярные модификации реакции на сегодняшний день: двухфазная и трехфазная. В классической трехфазной реакции используется: щелочной раствор перекиси водорода, раствор алкена в водонерастворимом орг. растворителе (толуол, гексан) и нерастворимый пептид-катализатор. В двухфазной модификации, популярной в последние годы, используется комплекс перекиси водорода с мочевиной и ДБУ в качестве основания. При этом реакция проводится в ТГФ, где катализатор почти не растворим.
Механизм реакции плохо изучен, единственный на данный момент постулированный механизм предполагает что реакция протекает через стадии бысторго обратимого присодинения гидропероксид аниона и последующую медленное внутримолекулярное нуклеофильное замещение гидроксида, ведущее к эпоксиду. . Стереоселективность реакции обеспечивается тем, что полилейцин координирует с интермедиатом 3, обеспечивая необходимую для циклизации геометрию, и стабилизируя сам интермедиат. Электронакцепторный эффект, образующегося в реакции эпоксида уменьшает способность карбонила к образованию водородных стадий и ведет к освобождению продукта 2. |
|
Общая методика (J. Chem. Soc., Perkin Trans. 1, 1998, 3171–3179 ссылка): Енон (0.24 ммоль), ДБУ (3 капли) и мочевина–H2O2 (27 мг, 0.28 ммоль, 1.2 экв.). были добавлены к суспензиии иммобилизованного поли-L-лейцина (100 мг) в ТГФ (0.8 мл). Реакционную смесь перемешивали при комнатной температуре, прохождение реакции контролировали по ТСХ (20% EtOAc– легкий петр. эфир). (В тех случаях, когда реакция не завершаоась в течении 16 часов, к реакционной смеси добавлялось дополнительное количество мочевины–H2O2 (27 мг, 0.28 ммоль, 1.2 экв.). Реакционную смесь разбавили этилацетатом (1 мл) и поли-L-лейцин отфильтровали, промыв дополнительно EtOAc. Фильтрат промыли водой (3 × 10 мл), высушили над MgSO4 и сконцентрировали в вакууме. Полученное коричневое масло очистили колоночной хроматографией (силикагель/0–15% EtOAc – легкий петр. эфир). Выхода от средних до хороших. |
|
Ссылки: 1. Первая публикация: Colonna et al., Org. Synth.; Mod. Trends, Proc. IUPAC Symp. 6th, 1986, 275; S. Julia, J. Masane, J. Carlos, Angewandte Chemie Int. Ed. Engl., 1980, 19, 929. 929-31. 2. Обзоры: (a) C. Lauret, S.M. Roberts, Aldrichimica Acta 2002, 35(2), 47-51. link (b) D. R. Kelly, S. M. Roberts, Biopolymers (Peptide Science), 2006, 84, 74–89, link. 3. Механизм: D. R. Kelly, S. M. Roberts, Chemical Communications 2004, 18, 2018-2020. |
|
Использование Реакции Жюлиа-Колонна в современной литературе: |
|
Примечания: Реакция Жюлиа-Колонна была использована для синтеза энантиомерночистого эпоксида 1 (> 98 %ee), ключевого исходного для синтеза клаусенамида ((+)-clausenamide), антиамнестического препарата с потенциальной гепатозащитной активностью. Ссылки: M. W. Cappi, W.-P. Chen, R. W. Flood, Y.-W. Liao, S. M. Roberts, J. Skidmore, J. A. Smith, N. M. Williamson, Chemical Communications 1998, (10), 1159-1160. link
|
|
Примечания: Ссылки: |