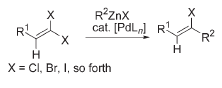|
Негиши Реакция (Negishi Crosscoupling) спасибки мне и неизвестным щвейцарцам |
|
|
Сочетание открытое Негиши в 1977 году было первой реакцией позволяющей получить несимметричные арилы с хорошими выходами. Удобное никель- или палладийкатализируемое сочетание цинкорганических соединений с разнообразными галогенидами (арил, винил, бензил или аллил) имеет широкий спектр применений, и сегодня уже не ограничевается синтезом биарилов. |
|
|
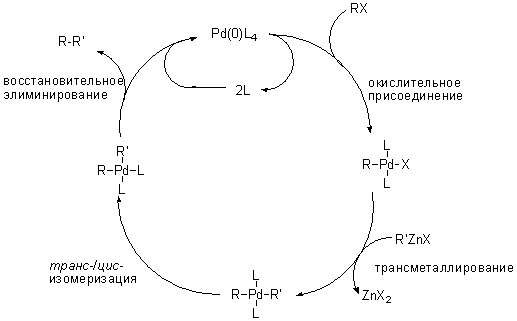
Схема и механизм:
R = винил, арил, бензил, аллил R = винил, арил, бензил, аллил, алкил cat. = Ni(PPh3)4, Pd(PPh3)4, и т.д.. X = Cl, Br, I для Ni-катализаторов., и Br, I для Pd-катализаторов. Также как и для других палладий и никель катализируемых сочетаний постулированный механизм включает: окислительное присоединение, трансметаллирование и восстановительное элиминирование приводящее к продукту. Предполагается, также что транс-/цис- изомеризация палладиевого комплекса одна из ключевых стадий.
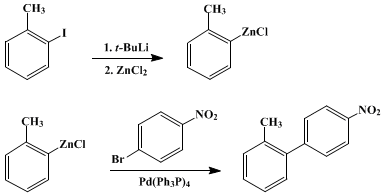
Пример реакции:
|
|
|
Общая методика: Organic Syntheses, Coll. Vol. 8, p.430 (1993); Vol. 66, p.67 (1988). ссылка
2-Метил-4'-нитробифенил. К смеси 1.16 г (1 ммоль) тетракис(трифенилфосфин)палладия, 100 мл тетрагидрофурана и 20.2 г (100 ммоль) 1-бром-4-нитробензола помещенных в 500 мл колбу был добавлен раствор о-толилцинкхлорида при охлаждении водяной баней. Реакционную смесь перемешивали в течении 6 часов при комнатной температуре, по окончанию реакции смесь вылили в колбу с 100 мл эфира и 300 мл ледянной 3 N соляной кислоты. Органический слой был отделен, а водный проэкстрагирован двумя 100 мл порциями эфира. Объединенные органические фазы были промыты насыщенным раствором гидрокарбоната натрия и высушены над безводным сульфатом магния. Осушитель был отфильтрован и растворитель удален в вакууме роторного испарителя. Продукт выделен в виде светло-коричневого твердого остатка, который был перекристаллизованы из 300 мл гексана. После первой кристаллизации получено 16 г. желтых игл, вторая кристаллизация остатков из 50 мл гексана дает дополнительные 2.4 г. в-ва. Перекристаллизация маточника из 100 мл этанола дает еще 0.5 г дополнительно Общий выход 2-метил-4'-нитробифенила 16.5 г. (78% по 1-бром-4-нитробензолу). |
|
|
Ссылки: 1. Первая публикация: Negishi, E.; Baba, S. J. Chem. Soc., Chem. Commun. 1976, 597. 2. Обзоры: (а) Negishi, E.; Anastasia, L. Chem. Rev. 2003, 103, 1979. (б) P. Knochel. R.D. Singer, Chem. Rev. 1993, 93, 2117-2188. 3. Механизм: |
|
|
Использование Реакции Негиши в современной литературе: |
|
|
Примечания: 1,1-дигалоген-1-алкены могут быть селективно превращены в транс-алкены посредством высоко селективного палладий катализируемого сочетания. Ссылки: Angew. Chem. Int. Ed. 2006, 45, 762 –765 |
|
|
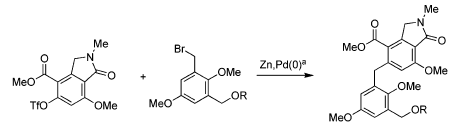
Примечания: Сочетание Негиши было применено для синтеза алкалоида Лактонамицина. Ссылки: Wehlan, H.; Jezek, E.; Lebrasseur, N.; Pave, G.; Roulland, E.; White, A. J. P.; Burrows, J. N.; Barrett, A. G. M. J. Org. Chem.; 2006; 71(21); 8151-8158. |
|