|
Асимметрическое эпоксидирование по Шарплессу (Sharpless asymmetric epoxidation) спасибки yimon aye |
|
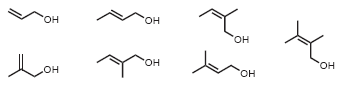
- это энантиоселективное эпоксидирование аллильных спиртов с использованием катализатора на основе титана. Наболее часто используемые реагенты: Ti(OiPr)4 в качестве катализатора, tBuOOH в качестве окислителя и (+) или (-) диэтилтартрат в качестве хирального лиганда, т.к. он наиболее удобен с точки зрения доступности обоих энантиомеров и легко предсказуемой стереоселективности.
|
|
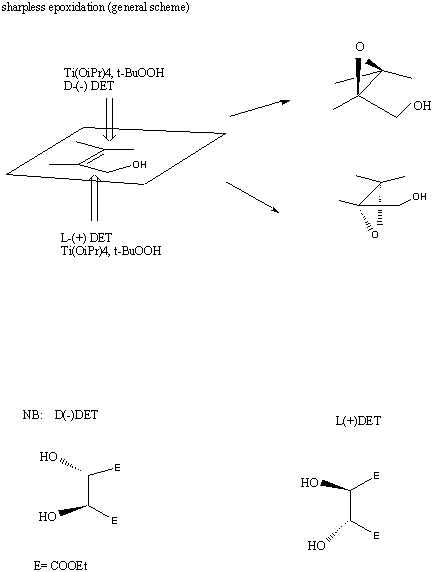
Схема и механизм
Пример реакции: При переходе от одного энантиомера тартрата к другому в качестве катализатора приводит к другому энантиомера продукта:
Общая методика для асимметрического эпоксидирования прохиральных аллиловых спиртов. В колбу из сушильного шкафа с сухой мешалкой были помещают аллиловый спирт (1 .0 экв), и диалкил тартрат (1.2 экв. ). Колбу оборудуют септой и наполняют аргоном. Абсолютный хлористый метилен добавляют в инертной атмосфере шприцем и охлаждают до 0 °C или -20 °C перед добавлением тетраалкоксида титана. (1.0 зквив.). NВ: рекомендуется использовать порошок активированных 3-A молекулярных сит (0.2-0.4 г в 10 мл р-ра) для асимметрического гидроксилирования. По прошествии 15-30 мин добавляют терт-Бутилгидропероксид с помощью шприца (достаточно плотного и непроницаемого для газов) для иниациализации реакции. За реакцией следят по ТСХ, по окончании реакции избыток гидропероксида удаляют перемешиванием с водноым раствором винной кислоты (10% масс) насыщенного FeSO4. Пример методики: Organic Syntheses, Coll. Vol. 7, p.461 (1990); Vol. 63, p.66
(1985). ссылка |
|
Ссылки: 1. Первая публикация: T. Katsuki, K. B. Sharpless, J. Am. Chem. Soc. 1980,102, 5974. 3. Обзоры: (a) Pfenninger, A. Synthesis 1986, (2), 89-116. (b) Katsuki, Tsutomu; Martin, Victor S.Organic Reactions 1996, 48, 1-299. |
|
Асимметрическое эпоксидирование по Шарплессу в современной литературе: |
|
Примечания: Стереоселективный синтез природных производных октадекадиенкарбоновой кислоты, выделяемыми рисом для борьбы с грибками вызывающими пирикуляриоз, был осуществлен с использованием асимм. эпосксидирования по Шарплессу. При введении в реакцию рацемического дивинмлового спирта был выделен только один энантиомер эпоксида, второй непрореагировавший энатиомер спирта был возвращен с 57 % выходом. Ссылки: T. Honda, M. Ohta, H. Mizutani, J. Chem. Soc., Perkin Trans. 1: Organic and Bio-Organic Chemistry 1999, (1), 23-30. |
|
Примечания: Эпоксидирование по Шарплессу было использовано на ранних стадиях в синтезе полиэфирного антибиотика ferensimycin B. Ссылки: Evans, D. A.; Polniaszek, R. P.; DeVries, K. M.; Guinn, D. E.; Mathre, D. J. J. Am. Chem. Soc. 1991, 113, 7613-7630. |

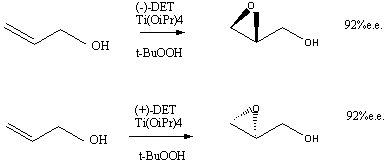
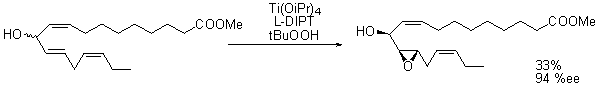
 76%
(90 e.e.)
76%
(90 e.e.)