Сочетание Стилле (Stille Coupling)
a summary by Davey Stoker (Lincoln)
Сочетание арил- и винил- производных катализируемое палладием. Будучи впервые опубликованным в семидесятые годы, сочетание Стилле является одним из наиболее используемых кросссочетаний. на сегодняшний день, на него приходиться до половины опубликованных реакций данного типа. Механизм включает в себя: a)Oкислительное присоединение арил- или винил- галогенида/трифлата с образованием палладийорганического интермедиата I.b) Последуюшие трансметаллирование с арил или винилстаннаном дает комплекс II. c) Восстановительное элиминирование от палладийорганического интермедиата II высвобождает продукт сочетания и катализатор Pd(0).
Дополненние: Трифлаты как правило более доступны для сочетания, чем соответствующие галогениды, т.к. могут быть легко синтезированы из соответствующих фенолов или енолизируемых альдегидов и кетонов. Внутримолекулярное сочетание Стилле с алкинилстаннанами было использовано для синтеза средних и больших карбоциклов в работах Николау. Хлорангидриды могут быть также использованы для сочетания с винил или арил станнанами в атмосфере СО для предотвращения декарбонилирования. Также стоит отметить что при проведении реакции в присутствии СО могут быть получены продукты карбонилирования.
Общая схема и механизм:
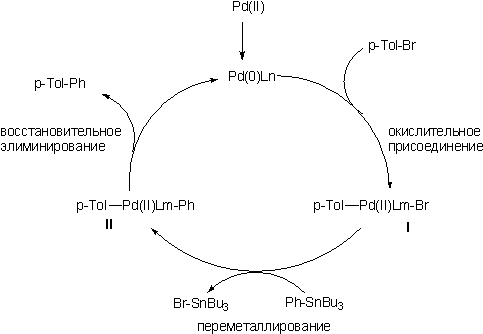
Пример:
Данный примере реакция Стилле была использована для полного синтеза каразостатина, гиеллазола и карбоазокиноцинов B-F группой японских химиков 2. Сочетание Стилле между 3-йодиндолом и винилстаннаном было ключевой стадией данного синтеза. Сочетание Сузуки было также использовано в данном синтезе.
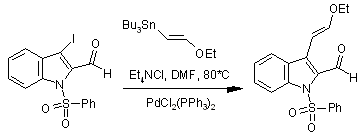
Organic Syntheses, Coll. Vol. 10, p.9 (2004); Vol. 77, p.135 (2000). ссылка
Organic Syntheses, Coll. Vol. 9, p.553 (1998); Vol. 71, p.97 (1993). ссылкаСсылки:
1. Первая публикация: Scott, W.J.; Crisp, G.T.; Stille, J.K. J. Am. Chem. Soc., 1984, 106, 4630
2. Choshi, T.; Sada, T.; Fujimoto, H.; Nagayama, C.; Sugino, E.; Hibino, S.* J. Org. Chem., 1997, 62, 2535-2543
3. Обзоры: Farina, V.; Krishnamurthy, V.; Scott, W. J. Organic Reactions 1998, 50, 1–652
4. Механизм:
Сочетание Стилле в современной литературе:
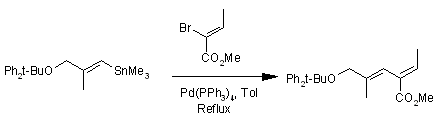
Комментарии: Полный синтез (+)-эполактена (epolactaene), нейритогенное (? neuritogenic) вещество выделенное из Penicillium sp. BM 1689-P и активного в клетках нейробластомы человека, был осуществлен с помощью сочетания Стилле. Конфигурация продукта сочетания была подтверждена посредством NOE-ЯМР (ЯЭО).
Ссылки: Marumoto, S.; Kogen, H.;* Naruto, S.* J. Org. Chem., 1998, 63, 2068-2069.
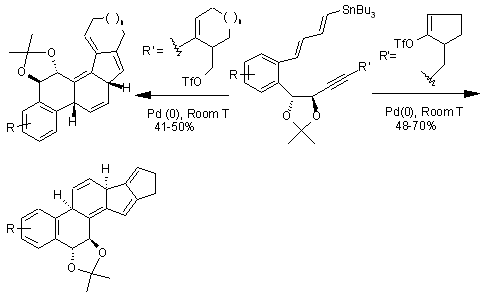
Комментарии: Хороший пример использования внутримолекулярной реакции Стилле алкинил станнанов для синтеза полициклических соединений. Сочетание Стилле последуют две последовательных циклизации по Дильс-Альдеру ведущие к желаемому продукту. В статье рассмотрены примеры использования разнообразных исходных (отличающихся R и R').
Ссылки: Bruckner S., Abraham E., Klotz P., Suffert J.Organic Letters., 2002, 4 (20): 3391-3393
другие современные именные реакции
на главную