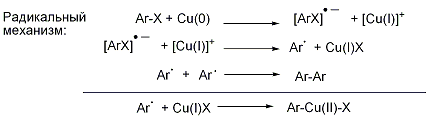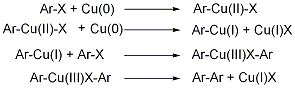|
Реакция Ульмана II (Ullmann reaction) возм.синонимы: сочетание Ульмана спасибки мне |
|
|
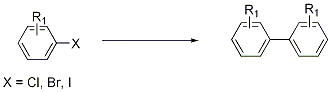
В современной литературе под реакцией Ульмана подразумевается несколько реакций проводимых с помощью меди или ее соединений: - гомосочетание арилгалогенидов или гетерарилгалогенидов. - арилирование фенолов, аминов, амидов (Голдберга модификация), тиофенолов, сульфиновых кислот, более подробно рассмотрено тут. Сочетание арилогалогенидов как правило осуществляют при высоких температурах >100 °C , в присутствии порошковой меди или бронзы. Возможно использование Cu2O, Cu2S но выхода ниже. Сочетание арилгалогенидов в присутствии меди было опубликовано Ф. Ульманном в 1901 году. Реакция представляет собой удобный метод синтеза обширного класса органических соединений. |
|
|
Спектр применения и ограничения: - Реакционная способность I > Br > Cl - Реакция практически не применима для синтеза несимметричных биарилов. - Реакция плохо применима для сочетания фенолов или незамещенных анилинов. Схема и механизм: Механизм реакции Ульмана известен весьма примерно. Предполагаются два возможных механизма реакции: радикальный механизм и с промежуточным образованием медьорганических соединений. Ни один из указанных механизмов нельзя исключить полностью и возможно, что большинство реакций протекает по обоим путям.
Второй механизм с промежуточным образованием медьорганических соединениями без участвия радикалов представлен ниже. Многие соединения типа Ar-Cu стабильны и дают при нагреве биарилы.
При реакциях в присутствии солей меди (I) всегда реализуется второй механизм. |
|
|
Показательные Методики: Organic Syntheses, Coll. Vol. 3, p.339 (1955); Vol. 20, p.45 (1940). link |
|
|
Ссылки: 1. Первая публикация: F. Ullmann, J. Bielecki, Berichte der deutschen chemischen Gesellschaft, 1901, 34 (2), 2174 - 2185. 2. Обзоры: (a) J. Hassan, M. Sevingnon, C. Gozzi, E. Shulz, M. Lemaire, Chem. Rev. 2002, 102, 1359 – 1469. (б) P.E. Fanta Chem. Rev., 1964, 64 (6), 613–632. (в) T. D. Nelson, R. D. Crouch Organic Reactions Vol. 63, 265-555. 3. Механизм: (а) S. E. Douglass, S. T. Massey, S. G. Woolard, R. W. Zoellner Transition Metal Chemistry, 1990, 15(4), 317-324. (в) T. D. Nelson, R. D. Crouch Organic Reactions Vol. 63, 265-555. |
|
|
Использование реакции Ульмана в современной литературе: |
|
|
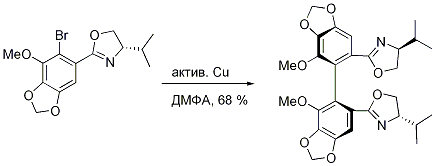
Примечания: При синтезе природного соединения wuweizisu C из галловой кислоты была использована реакция Ульмана. .Ключевая стадия (см. схему) построения асимметрической оси была осуществлена с помощью сочетания Ульмана. Продукт, стереохимия которого определялась стереохимией оксазолина, был получен с 68%ым выходом и >99% de. Бифенол с противоположной конфигурацией был получен с использованием оксазолина противоположной конфигурации. Ссылки: Y. Li, Q. Wang, L. Dong, X. Guo, W. Wang, J. Xie, J. Chang Synthesis 2009(20): 3383-3390. |
|
|
Примечания: Сочетание Ульмана было использовано на ключевой стадии получения серии новых бидентантного лигандов для палладий-катализируемого гидрирования. Биарил получен с 96ти %ым выходом при нагревании исходного бромида с медью в ДМФА. Ссылки: as: Wang, C., Yang, G., Zhuang, J., Zhang, W., Tetrahedron Letters 2010, doi: 10.1016/j.tetlet.2010.02.055 |
|