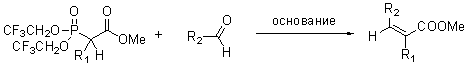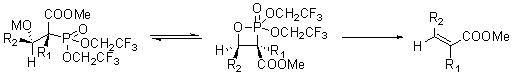|
Реакция Стилл-Геннари (Still-Gennari olefination) спасибки мне |
|
Реакция Стилл-Геннари является крайне популярной модификацией реакции Хорнера-Вадсворта-Эммонса (HWE) и наиболее эффективной методикой получения Z-олефинов из альдегидов. |
|
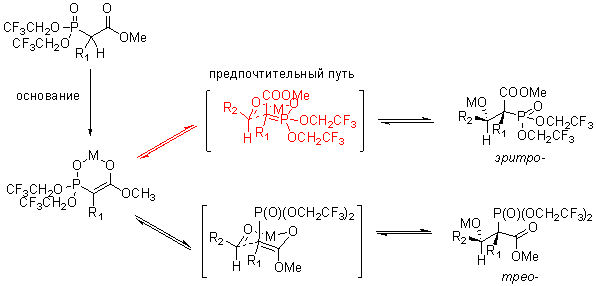
Схема и механизм:
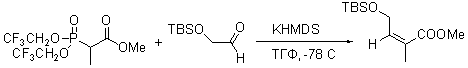
R1 = H, алкил R2 = алкил, арил основание = KHDMS, 18-краун-6. Природа заместителей при стаблизированном фосфонатном карбанионе может значительно влиять на стереохимию продуктов реакции с альдегидами. бис-(2,2,2-трифторэтильные) заместители на фосфоре полностью меняют обычную для реакции стереохимию продуктов. В реакции Стилл-Геннари вместо обычных для HWE реакции (E)-алкенов получаются почти исключительно (Z) олефины. Т.к. заместители существенно ускоряют скорость элиминирования фосфиноксида ведущую к алкену, что подавляет образование термодинамически более выгодных (E)-алкенов.
|
|
Общая методика. Получение реагента: Organic Syntheses, Coll. Vol. 9, p.88 (1998); Vol. 73, p.152 (1996). ссылка |
|
Ссылки: 1. Первая публикация: Still, W.C.; Gennari, C., Tetrahedron Letters, 1983, 24, 4405. 2. Обзоры: (a) M. Edmonds, A. Abell, Modern Carbonyl Olefination 2004, 1-17. (б) Motoyoshiya, Jiro. Recent developments in Z-selective Horner-Wadsworth-Emmons reactions. Trends in Organic Chemistry 1998, 7 63-73. 3. Механизм: K. Ando, J. Org. Chem. 1999, 64, 6815-6821; (b) P. Brandt, P.-O. Norrby, I. Martin, T. Rein, J. Org. Chem. 1998, 63, 1280-1289. |
|
Использование реакции Стилл-Геннари в современной литературе: |
|
Примечания: Synthesis of migrastatin and its macrolide core. Ссылки: S. Reymond, J. Cossy, Tetrahedron 2007, 63(26), 5918-5929. |
|
Примечания: Реакция Стилл-Геннари была использована для синтеза важного исходного в синтезе антибиотика ансатриенола. Трехзамещенный олефин был получен с 71 % выходом с абсолютной стереоселективностью. Ссылки: D. Kashin, A. Meyer, R. Wittenberg, K.-U. Schoening, S. Kamlage, A. Kirschning, Synthesis 2007, (2), 304-319 |