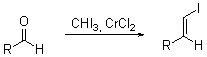|
Такая Реакция (Takai reaction) (возможные синонимы: Такай реакция, Такаи реакция) спасибки мне и |
|
Реакией Такая называют превращение альдегидов в транс-винилйодиды под воздействием йодоформа и солей хрома (II). Возможно использование также хлороформа и бромоформа для превращения в соответствующие винилгалогениды. В сочетании с реакцией Нозаки представляет собой мощный метод синтеза природных соединений. |
|
Схема и механизм: R = Ar, Alk и т.д. Растворитель: ТГФ, диоксан. В реакцию вступают также кетоны, но реакция происходит намного медленее и позволяет провести первращение в альдегидной группы в присутствии кето-группы. При превращениях кетонов выхода реакции редко превышают 50%.
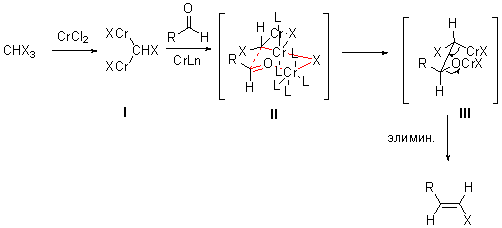
Постулированный механизм предполагает образование геминального хромового реагента I из галоформа и хлорида хрома. Данный интемедиат присоединяется к альдегиду по карбонильной группе с образованием хромового интермедиата II, присоединение происходит через шестичленное циклическое перреходное состояние с мостиковым атомом галогена. Последующие син-элиминирование (LnCr)2O происходит легко и вращение по двойной связи не успевает произойти. Это позволяет получить E-олефин с высокой стереоселективностью.
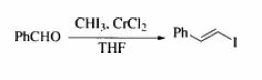
Пример реакции:
|
|
Общая методика: (E)- β -Йодстирол [Синтез E- Алкенил галогенидов из Альдегидов] К суспензи безводного хлорида хрома(II) (0.74 г, 6.0 ммоль) в ТГФ (10 мл) при 0° был добавлен по каплям раствор бензальдегида (0.11 g, 1.0 mmol) и йодоформа (0.79 г, 2.0 ммоль) в ТГФ (5 мл). Смесь перемешивали при 0° в течении 3 часов, затем вылили в воду (25 мл) и экстрагировали эфиром (3 × 10 мл). Обьединенные органические экстракты высушили над сульфатом натрия, отфильтровали и упарили в вакууме. Продукт был выделен после колоночной хроматографии в виде бесцветного масла 0.20 г (87%, E:Z = 94:6). IR (neat): 3056, 2920, 1595, 1494, 1169, 1069, 946, 726 cm–1; 1H NMR ( CDCl3): δ 6.89 (d, J = 15 Hz, 1H), 7.30–7.53 (m, 5H), 7.49 (d, J = 15 Hz, 1H). Соединения низковалентного хрома, получаемые при восстановлении хлорида хрома (III) (6.0 ммоль) алюмогидридом лития (3.0 ммоль) могут быть использованы вместо хлорида хрома(II). Использование смеси растворителей диоксан-ТГФ (6:1), иногда дает лучшую стереоселективность чем ТГФ в случае алифатических альдегидов. |
|
Ссылки: 1) Первая публикация. K. Takai et al., J. Am. Chem. Soc. 1986, 108, 7408.2) Обзоры: Korotchenko, V. N.; Nenajdenko, V. G.; Balenkova, E. S.; Shastin, A. V. Russian Chemical Reviews 2004, 73(10), 957-989; В.Н. Коротченко, В.Г. Ненайденко, Е.С. Баленкова, А.В. Шастин, Успехи Химии, 2004, 73(10), 1039-1074; (b) Takai, Kazuhiko. Addition of organochromium reagents to carbonyl compounds. Organic Reactions (New York) 2004, 64 253-612. 3) Механизм: Hodgson, D. M.; Boulton, L. T.; Maw, G. N. Tetrahedron Lett. 1994, 35, 2231; Takai, K.; Shinomiya, N.; Kaihara, H.; Yoshida, N.; Moriwake, T.; Utimoto, K. Synlett 1995, 963. |
|
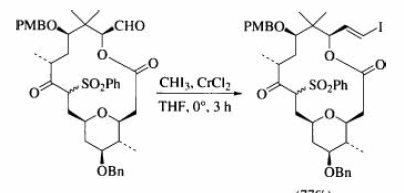
Использование Реакции Такая в современной литературе: |
|
Примечания: Так как кетогруппа намного менее реакционноспособна чем альдегидогруппу, то альдегид может быть селективно превращен в алкен. Сложные эфиры, лактоны, амиды, нитрилы, сульфоны так же сохраняются нетронутыми. Ссылки: Paquette, L. A.; Barriault, L.; Pissarnitski, D. J. Am. Chem. Soc. 1999, 121, 4542. |
|
Примечания: Ссылки: |