Юлия Реакция (Julia Olefination) (возм. синонимы Жюлиа, Юлия - Литго)
спасибки Rob Martin
Схема и механизм:
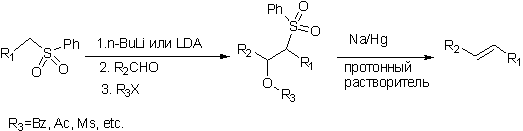
Синтез алкенов по Юлия это многостадийное превращение: первая стадия это генерация стабилизированного карбоаниона из сульфона и последующее присоединение его к карбонильной группе. Образующийся спирт превращают в бензоат, ацетат или мезилат, которые в свой очередь в присутствии амальгамы натрия превращаются в Е-алкены с высокой стереоселективностью. В некоторых случаях образующиеся спирты могут быть восстановлены амальгамой натрия в алкены напрямую.
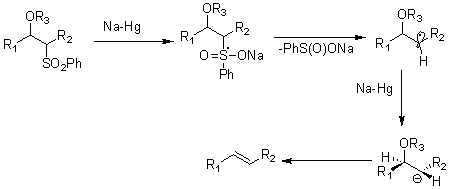
Геометрия конечного алкена не зависит от стереохимии исходного бета-гидроксисульфона т.к. образующийся на стадии восстановительного элиминирования промежуточный анион 2 довольно стабилен и успевает приобрести наиболее термодинамически выгодную транс-конфигурацию до отщепления карбоксилат-иона.
- В случае синтеза три- и тетразамещенных алкенов выхода невысоки.
- Для получения трехзамещенных алкенов предпочтительно сочетание дизамещенных сульфонов с альдегидами (а не кетонов).
- Амальгаму натрия можно заменить магнием, йодидом самария.
Разработана также одностадийная модификация реакции Жюлиа, известная как реакция Жюлиа-Кочиенски.
Пример реакции:
На первой стадии происходит присоединение аниона сгенерированного из фенилсульфона к карбонильной группе. Дальнешая обработка продукта присоединения амальгамой натрия ведет к потере арилсульфонильной группы и к генерации карбаниона. Интермедиат довольно стабилен и при свободном вращении принимает наиболее стабильную конформацию, которая после элиминирования ведет к E-алкену. Сульфоны с большими заместителями ведут к улучшению соотношения E:Z изомеров.
Пример методики:
Ссылки:
1. Первая публикация: M. Julia, M.-M. Paris, Tetrahedron Letters 1973, 4833.
2. Обзоры: (а) Blakemore, Paul R. Journal of the Chemical Society, Perkin Transactions 1 2002, (23), 2563-2585. (б) R. I. Dumeunier, I. E. Marko, Modern Carbonyl Olefination 2004, 104-150. (в) D. Alonso, M. Fuensanta, C. Najera, M. Varea, Phosphorus, Sulfur and Silicon and the Related Elements 2005, 180(5-6), 1119-1131. (e) В. Н. Коротченко, В. Г. Ненайденко, Е. С. Баленкова, А. В. Шастин, Успехи Химии, 2004, 73(10), 1039-1074.
3. Механизм: R. I. Dumeunier, I. E. Marko, Modern Carbonyl Olefination 2004, 104-150.
Синтез алкенов по Юлия в современной литературе:
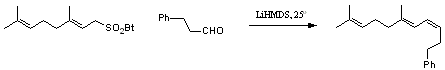
Примечания: Был продемонстрированн удобный подход к синтезу E,Z-диенов по реакции Юлия.
Ссылки: A.B. Charette et al, Tetrahedron Letters 42, 2001, 5149-5153